Гальванический элемент батарейка -это энергетическое устройство, которое преобразует накопленную химическую энергию непосредственно в электрическую с помощью электрохимического процесса, включающего реакции окисления.
Каковы основные компоненты батареи как генератора энергии?
Гальванический элемент может состоять из многих электрохимических элементов, называемых батарейными элементами. Элементы или ячейки могут быть соединены и расположены последовательно или параллельно в соответствии с требуемым выходным напряжением и током, образуя емкость батареи.
Гальванический элемент батарейка состоит из трех основных компонентов:
- Анод (отрицательный электрод). Это восстановительный электрод, который отдает электроны во внешнюю электрическую цепь и окисляется в ходе электрохимической реакции. Таким образом, анодные электроды также называют “топливным электродом».
- Катод (положительный электрод). Катод-это окислительный электрод, который принимает электроны от внешней цепи и восстанавливается в ходе электрохимической реакции.
- Электролит (электродная среда). Электролит представляет собой среду или сепаратор между анодом и катодом, который служит ионным проводником для переноса ионов или зарядов между двумя электродами. Обычно это жидкость с кислотами или щелочами для придания ионной проводимости.
Необходимо отметить, что некоторые батареи используют твердые электролиты, поэтому мы обычно называли их “сухими ячейками” или “сухими батареями».
Первые компоненты типичного сухого элемента в качестве анода использовали цинк, а в качестве катода-графитовый (углеродный) стержень, окруженный влажным электролитом (химическая смесь).
Другие более современные распространенные сухие гальванические элементы батарейки включают цинк-хлоридные, ртутные, оксид серебра, цинк-воздушные батареи и т. д.
Классификация источников питания
Как правило, батареи можно разделить на первичные, вторичные и топливный элемент.
Первичные батареи не могут быть заряжены, в то время как вторичные являются перезаряжаемыми или аккумуляторами.
В отличие от первичных и вторичных батарей, топливные элементы, с другой стороны, относятся к классу которые работают с непрерывной внешней подачей топлива.
Поэтому количество энергии для первичной батареи ограничено имеющимися в ней реагентами; вторичная может работать в прерывистом режиме, т. е. она может быть перезаряжена при достижении низкого уровня заряда.
Топливный элемент, по существу, имеет наибольшее количество энергии, так как топливо, обычно водород, может непрерывно подаваться в “топливный” элемент.
Марганцево-цинковый сухой элемент или угольно-цинковая батарейка
Гальванический элемент батарейка электролитом которого является сухой или в форме пасты/геля был изобретен французский инженером Жоржем Лекланшем в 1866 году.
Стаканчик из цинка – минусовой электрод, электролитом служил диоксид марганца, графитовый электрод в качестве плюсового электрода.
Электрохимическая реакция Zn + 2MnO2 + 2NH4Cl → 2MnO(OH) + [Zn(NH3)2]Cl2
Применяются солевые батарейки в приборах со средним и низким энергопотреблением.
Щелочная (алкалиновая) батарейка
Щелочной диоксид цинка-марганца или ”щелочной» гальванический элемент батарейка обеспечивает гораздо более высокую плотность энергии и, следовательно, емкость, чем углерод-цинковый или марганцево-цинковый-хлоридный тип. Она также способна к более высокому разрядному току. 
Диоксид марганца (MnO2) и углерод образуют положительный электрод, в то время как цинк находится в порошкообразной форме, как отрицательный электрод (анод), который фактически смешивается с образованием геля/пасты с гидроксидом калия (KOH) с цинковым порошком в качестве электролита. Несмотря на то, что щелочная батарея дороже и несколько тяжелее, она превосходит углерод-цинковые или хлоридные типы. Кроме того, щелочные батареи, как известно, долговечны из-за их способности избегать коррозионного воздействия из-за кислого иона аммония на цинк. Щелочные гальванические элементы батарейки особенно подходят для применений, которые включают в себя сравнительно высокие уровни тока разряда.
Литиевая батарейка
Литий-марганцевая диоксид батарейка -это относительно недавняя разработка, использующая преимущества высокого электродного потенциала и плотности энергии металлического лития. Она предлагает значительно большую плотность энергии и емкость, чем “щелочная” и угольная, при относительно небольшом увеличении стоимости.
Литий находится в форме очень тонкой фольги и запрессован внутри банки из нержавеющей стали, чтобы сформировать отрицательный электрод.
Положительный электрод — диоксид марганца, смешанный с углеродом для улучшения его проводимости, а электролит-перхлорат лития растворен в пропиленкарбонате.
Номинальное напряжение на клеммах литиевого элемента составляет 3,0 в, что в два раза больше, чем у “щелочных” и других гальванических элементов. Он также имеет очень низкую скорость саморазряда, что дает ему очень длительный срок хранения. Внутреннее сопротивление также довольно низкое и остается таким в течение всего срока службы.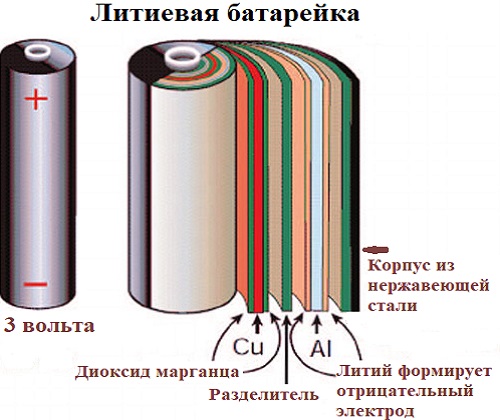
Литиевая батарея хорошо работает при низких температурах, даже ниже -60 °C, и передовые разработки используют их в спутниках связи, космических аппаратах, военных и медицинских приложениях. Медицинские приложения, требующие длительного срока службы критически важных устройств, таких как искусственные кардиостимуляторы и другие имплантируемые электронные медицинские устройства, используют специализированные литий-ионные батареи, которые могут работать в течение многих лет.
Литиевые гальванические элементы батарейки подходят для менее важных применений для работы с игрушками, часами и камерами. Хотя литиевые батареи стоят дороже, они обеспечивают более длительный срок службы, чем «щелочные» батареи, и сводят к минимуму их замену.
На практике, однако, напряжение на клеммах уменьшается по мере уменьшения заряда. Именно по этой причине, в отличие от вторичных батарей, первичные, как правило, не получают спецификации емкости ни в ампер-часах, ни в миллиампер-часах от большинства производителей вместо этого обычно задается только максимальный ток разряда.
Литиевые гальванические элементы обладают значительно большей плотностью энергии и емкостью, чем “щелочные” и другие первичные батареи; они обеспечивают более высокое (примерно в два раза) напряжение на клеммах по сравнению с другими первичными элементами, и напряжение на клеммах остается почти постоянным в течение всего срока службы.
Преимущества и недостатки применения гальванических элементов батареек
Преимущества
- Как эффективный и дешевый резервный генератор энергии.
- Компактный и удобный источник энергии для повседневного использования.
Недостатки:
- Не содержат много энергии.
- Отработанные источники вносят свой вклад в загрязнение окружающей среды.
- Многие элементы содержат очень агрессивные электролиты, такие как гидроксид калия или едкий калий.
- Некоторые батарейки содержат токсичные материалы, такие как оксид ртути или высокореактивные материалы, такие как литий, которые могут взорваться при контакте с водой.