В целом элементы периодической таблицы Менделеева можно разделить на металлы, неметаллы и металлоиды (полуметаллы).
Если смотреть по химическим свойствам, то видно, что несколько элементов иногда идентифицируются как металлоиды или полуметаллы и являются неметаллами, однако по типу проводимости являются проводниками.
Элементы металлоиды
Элементами, обычно признаваемыми металлоидами, являются бор, кремний, германий, мышьяк, сурьма и теллур.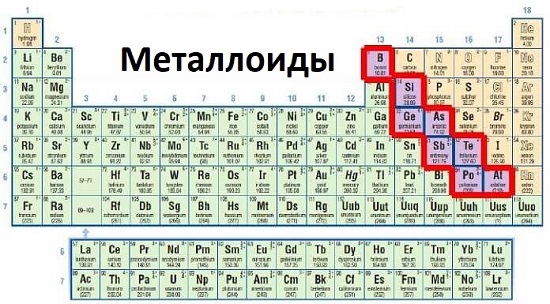
Некоторые элементы как переходные иногда классифицируют также: углерод, алюминий, селен, полоний и астатин.
Металлоиды находятся между металлами и неметаллами в периодической таблице. То, как эти элементы ведут себя при химических взаимодействиях с другими элементами, зависит главным образом от количества электронов на внешнем энергетическом уровне их атомов. Они могут действовать либо как металлы, либо как неметаллы в химических реакциях.
Большинство металлоидов обладают некоторыми физическими свойствами металлов и некоторыми физическими свойствами неметаллов. Они находятся между металлами и неметаллами по своей способности проводить тепло и электричество. Они блестящие, как металлы, но хрупкие, как неметаллы. Все они существуют в виде твердых тел при комнатной температуре.
Электрические полупроводники
Уже более 120 лет известно, что металлоиды имеют преимущественно неметаллическую химию. С появлением полупроводниковой промышленности в 1950-х годах и развитием твердотельной электроники с начала 1960-х годов металлоиды стали рассматриваться как “промежуточные элементы”. По большей части они считаются электрическими полупроводниками и сильно зависят от концентрации примесей, температуры и воздействия различных видов излучения.
Как самые слабые из неметаллов, им присваиваются положительные степени окисления (отдают электроны) в их соединениях с неметаллами и отрицательные степени окисления (электроны смещаются к атому) в их соединениях с большинством металлов.
Писавший в начале истории интерметаллических соединений британский металлург Сесил Деш отметил, что “некоторые неметаллические элементы способны образовывать соединения с металлами явно металлического характера, и поэтому эти элементы могут входят в состав сплавов”. Он связал кремний, мышьяк и теллур, в частности, с элементами, образующими сплавы. Соединения кремния, германия, мышьяка и сурьмы с металлами, вероятно, лучше всего классифицировать как сплавы. Что касается бора, то бориды переходных металлов часто обладают большей проводимостью, чем исходный металл. Например, TiB2 в пять раз превосходит электропроводность титана холодного прессования.
Известно, что бор образует металлический, ковкий, экструдируемый и обрабатываемый сплав, имеющий состав Li5B4 и серебристый металлический блеск.
Металлоиды образуют солеподобные или ковалентные соединения с металлами. Их оксиды являются слабокислыми в зависимости от условий. Органические соединения металлоидов подпадают под определение металлоорганических соединений.
Металлоиды имеют энергию ионизации около 200 ккал/моль (837 кДж/моль) и значения электроотрицательности, близкие к 2,0.
Металлоиды, как правило, являются полупроводниками, хотя сурьма и мышьяк [полуметаллы с точки зрения физики] имеют электрическую проводимость, приближающуюся к проводимости металлов.
Селен и полоний подозревались как не участвующие в этой схеме, в то время как статус астатина (редкий элемент в земной коре) является неопределенным. Многие химики утверждают, что астатин будет полноценным металлом.
Организация металлов и неметаллов
Металлоиды имеют от трех до шести электронов на своем внешнем энергетическом уровне.
Бор, является единственным металлоидом, имеющим всего три электрона на внешнем энергетическом уровне. Он имеет тенденцию действовать подобно металлам, отдавая свои электроны в химических реакциях.
Металлоиды с более чем четырьмя электронами на внешнем энергетическом уровне (мышьяк, сурьма и теллур) имеют тенденцию действовать как неметаллы, получая электроны в химических реакциях. Те, у кого ровно четыре электрона на внешнем энергетическом уровне (кремний и германий), могут действовать как металлы или неметаллы, в зависимости от других элементов в реакции.
Углерод, промежуточный неметалл, является наиболее электропроводным и теплопроводным из неметаллов (как графит и алмаз соответственно). В то время как пограничное металлическое серебро, которое проявляет химию переходных металлов в своих более высоких, менее стабильных степенях окисления, является аналогом «два в одном» среди металлов. Фосфор, промежуточный неметалл, имеет ту же кристаллическую структуру, что и марганец переходного металла. Йод, как почти металлоид, имеет кристаллическую структуру, аналогичную структуре галлия, другого близкого металлоида. Ксенон в состоянии окисления образует бледно-желтый взрывоопасный оксид XeO4, в то время как осмий образует желтый сильный окисляющий оксид OsO4.



